流式细胞术在 2020 年欧洲血液学年会(EHA)上大放异彩
2020 年新冠疫情全球肆虐,但疫情并未阻挡血液界学者对学术研究和交流分享的热情。承载众多看点的第 25 届欧洲血液学协会(EHA)年会,在大家的期待中采用线上虚拟会议的模式如期举行。
作为欧洲血液学领域规模最大的国际会议,EHA 年会每年吸引来自全球 100 多个国家的上万名专业人士与会,一起分享、探讨有关血液学的创新理念及最新的科学和临床研究成果,能够登上 EHA 舞台,表示在血液学领域具有较高的学术水平。此次,陆道培医学团队有 3 项研究成果亮相 EHA 大会,向世界展示和分享陆道培医学团队最新科研成果。
研究一:使用 cCD79a 设门的多色流式可以有效监测 CD19-CAR-T 治疗 B-ALL 后 MRD,并且预测桥接移植的预后
第一作者流式细胞室陈曼医师的文章「Multicolor Flow Cytometry Panel with cCD79A Gating to Detect Minimal Residual Disease in Patients with B-Lymphoblastic Leukemia/Lymphoma Post Anti-CD19 CAR-T Therapy Bridging to Allo-HSCT」(胞浆 CD79a 抗体设门多色流式法监测 CD19-CAR-T 桥接异基因移植治疗难治复发急性 B 淋巴细胞白血病)(摘要号:S113)被选为口头发言。
陆道培医疗集团在 CD19 嵌合抗原受体 T(CD19-CAR-T) 细胞治疗急性 B 淋巴细胞白血病(B-ALL)中有丰富的经验,尤其是桥接异基因造血干细胞移植,挽救了无数难治复发患者生命。这类疾病的病情监测、疗效评价、预后评估中,流式细胞术(FCM)微小残留病变(MRD)检测技术起到不可或缺的作用。
但是常规的 B-ALL 的 MRD 多色流式检测方法均使用 CD19 设 B 细胞门,而 CD19-CAR-T 治疗后,由于 13-60% 的 MRD 阳性或者复发患者肿瘤细胞会或多或少丢失 CD19,故不再适合使用传统方案监测 MRD。以王卉主任、陈曼医师为代表的团队,探讨了陆道培医疗集团流式细胞室使用胞浆 CD79a(cCD79a)抗体设门多色流式细胞术检测 MRD 方法在 CD19-CAR-T 治疗中的有效性,并研究其在输注后桥接异基因移植(allo-HSCT)整个治疗过程中的评价疗效及监测预后的作用。
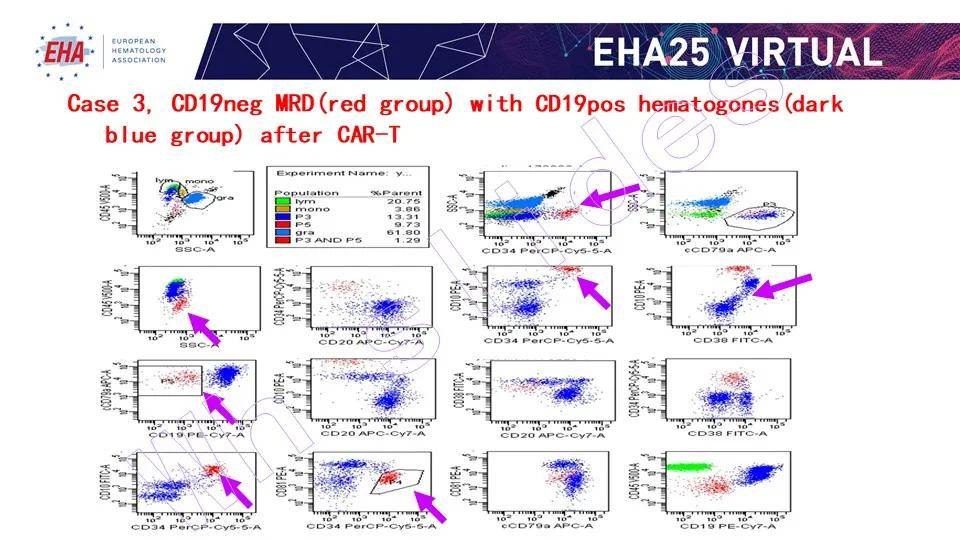
CD19-CAR-T 治疗后 CD19 阴性 MRD(红色细胞群为肿瘤细胞群)
实验中分别选取 10 例 B-ALL 完全缓解(CR)患者的骨髓标本及 10 例 B-ALL MRD 阳性的骨髓标本,同时使用新方案与经典方案进行检测,采用线性回归方法进行结果一致性分析,证实两种方案的一致性好。
然后选取 2016 年 6 月~2017 年 5 月于河北燕达陆道培医院经 CD19-CAR-T 细胞输注后桥接移植的 59 例患者,使用新方案进行骨髓 MRD 监测,中位随访 24 月。其中 51 例(86.44%)患者 CD19-CAR-T 后 FCM-MRD 阴性,8 例(13.56%)患者 CAR-T 细胞输注后 MRD 阳性或者复发。两组病例均在中位时间 1-2 个月左右进行了异基因造血干细胞移植。
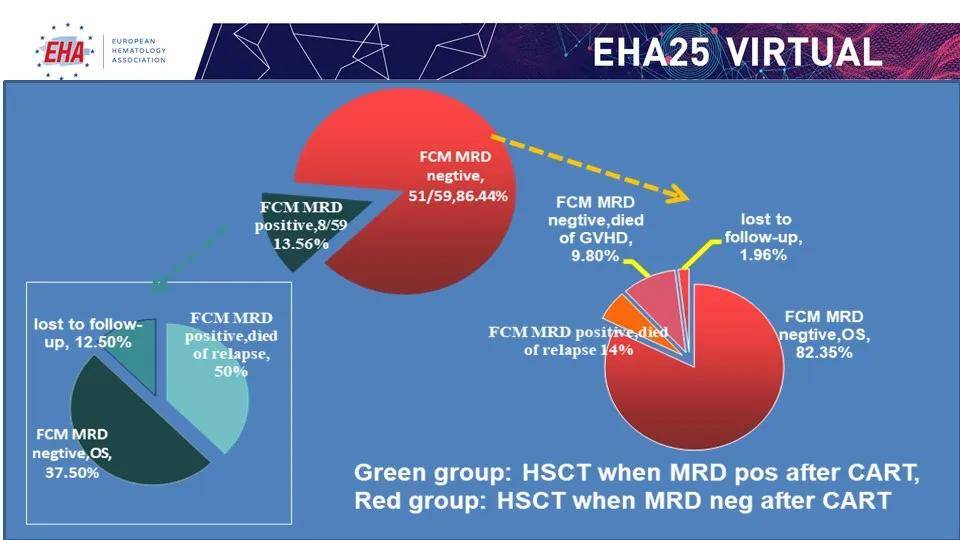
59 例患者的临床与预后情况
红色为 CD19-CAR-T 后 MRD 阴性移植组患者,绿色为 CD19-CAR-T 后 MRD 阳性带瘤移植组患者
经单因素卡方检验分析,CD19-CAR-T 后移植前以及移植后 FCM-MRD 均与移植预后有强相关性(分别为 P<0.0001,P = 0.000)。59 例患者中,移植后复发总计 9 例,其中 7 例死亡,4 例为移植前 FCM-MRD 阳性患者(占带瘤移植组 50%,4/8 例),3 例为 FCM-MRD 阴性移植患者(占 MRD 阴性移植组 5.88%,3/51 例),2 例复发后缓解均为移植前 FCM-MRD 阴性患者。
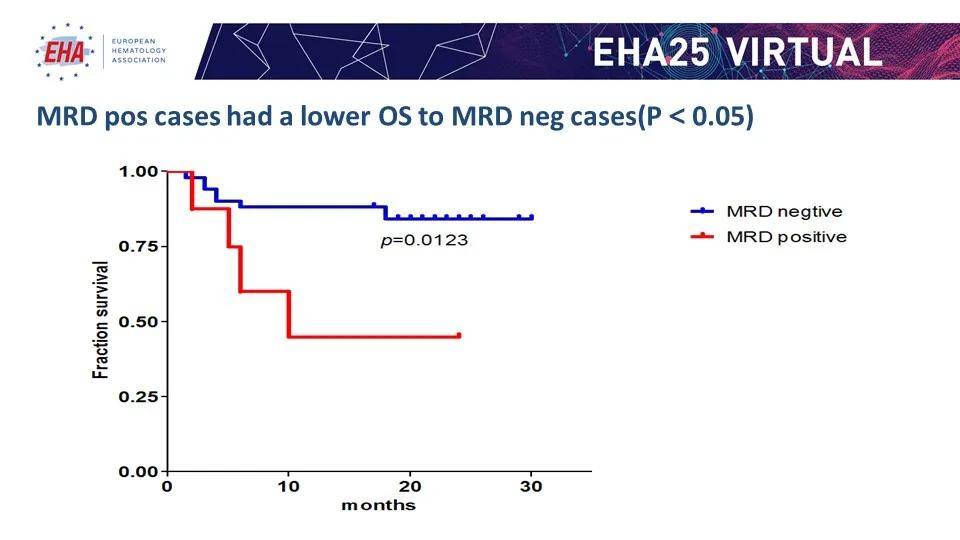
CD19-CAR-T 治疗后使用 cCD79a 方案多色流式检测 MRD 结果可以有效预测桥接移植后生存:MRD 阳性组预后差

结论认为,使用 cCD79a 设门的多色流式 B-ALL 检测 MRD 方案,可以有效监测 CD19-CAR-T 后 MRD,并且预测 CD19 CAR-T 后桥接移植的预后。
简介

陈曼医师,硕士研究生,主管检验技师、助理研究员。中国中西医结合学会检验学会流式细胞分析诊断专家委员会常务委员及秘书,北京医学检验医学专业委员会第一届血液学和体液学检验分会委员、北京中医药协会第三届中医检验专业委员会青年委员。
研究二:流式细胞术微球法检测 24 种细胞因子在 CAR-T 治疗中的应用
第一作者细胞冻存室王东出医师的文章「EP403 Monitoring 24 Cytokines by Cytometric Bead Array during the Chimeric Antigen Receptor T Cells Treatment」(流式细胞术微球法检测 24 种细胞因子在嵌合抗原受体 T 细胞治疗中的应用)被选为墙报展示。
研究表明在 CAR-T 治疗中,多种细胞因子在细胞因子释放综合征(CRS)或者细胞因子风暴中起到重要作用,因此细胞因子检测是评价 CAR-T 副作用的重要指标。流式细胞微球阵列技术(CBA)是最近发展起来的一项新技术,与传统的 ELISA 方法相比,具有灵活、快速、高性价比、节约标本等优点。以王卉主任、王东出医师为代表细胞冻存室团队设计了一项新的 24 种细胞因子组合方案,使用 CBA 方法评价了其在 CAR-T 患者的脑脊液和外周血细胞因子检测中的作用。
他们首先进行了方法学对照性研究,收集了 29 例健康志愿者的外周血,25 例回输 CD19-CAR-T 细胞后的 ALL 患者外周血标本,分别使用 ELISA(Quantikine,RND)检测四种常见细胞因子(IL-6、IL-10、IFN-γ、可溶性 CD25(sCD25)),与 CBA(北京旷博公司)方法进行了比较。结果表明,每种技术均有很好的重复性,两者相关性很好。
为了研究 CAR-T 后细胞因子变化曲线,研究者选取的 25 例 CAR-T 治疗患者每人至少采集了 5 个时间点。由于标本量的问题,ELISA 方法只做了正常对照和患者的外周血标本,CBA 方法除了检测外周血标本,还对 41 例未做 CAR-T 的完全缓解患者脑脊液标本和 15 例 CART 治疗后脑脊液标本进行了检测。
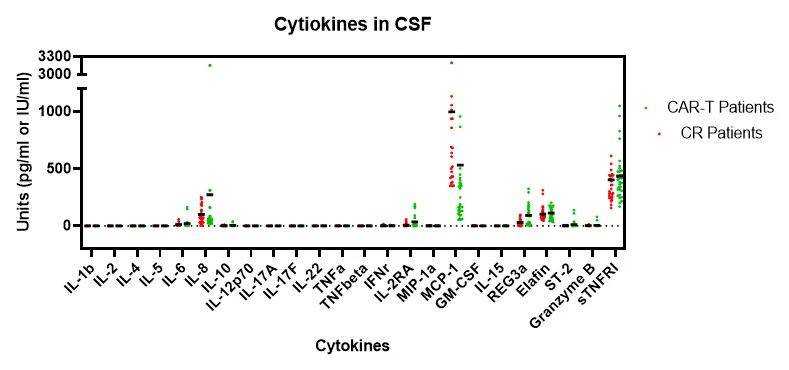
24 种细胞因子 CBA 方法检测 CD19-CAR-T 后脑脊液
绿色为对照组 CR 患者,红色为 CAR-T 患者
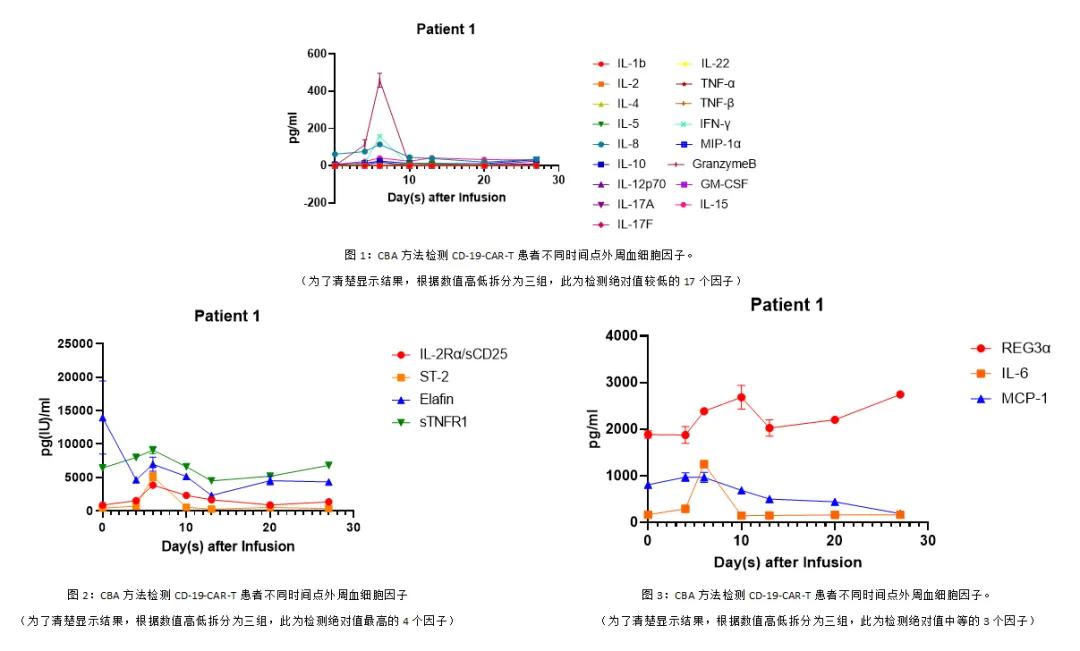
CBA 方法检测 CD19-CAR-T 患者不同时间点外周血细胞因子
结果表明,在健康对照和患者外周血标本组,虽然 IL-6 和 sCD25 检测的绝对值两种技术有差异,但是两种方法均可满意显示 CAR-T 治疗后细胞因子变化曲线,一致性很高。尤为重要的是,CBA 技术检测脑脊液和外周血均有临床实用性强的特点。CBA 方法可以一次完成 24 种细胞因子的检测,因此节约标本,让脑脊液这种微量标本检测成为可能;各种标本的检测中都解决了 ELISA 方法必须批量检测,随意性差的特点,相比之下检测时间短、性价比高,不论大批量还是急诊随机性标本都适合。
2020 年 2 月起,陆道培医疗集团已经将 CBA 方法 24 种细胞因子检测技术全面推向临床,这项技术不仅可用于 CAR-T 治疗患者的监测,同时在各种良、恶性疾病的诊断、治疗,感染的免疫指标评价,移植物抗宿主病、CMV、EBV 或者其他感染等移植后并发症的诊断、评价,噬血综合征等特殊免疫状态的监测与防治中,都起到极为重要的作用。
简介

陆道培医疗集团细胞冻存室王东出医师,University of Greenwich 硕士研究生,助理研究员。
研究三:CD69 在 AML 微小残留病变检测中的意义
第一作者流式细胞室宫美维医师的文章「The Clinical Significance of CD69 Detection in Minimal Residual Disease of Patiens with Acute Myeloid Leukemia」(CD69 在急性髓系白血病微小残留病变检测中的意义)被选为大会论文集。
微小残留病变(MRD)是恶性血液病重要的疾病监控、判断预后、指导治疗的指标,目前临床常用的灵敏度较高的检测方法包括实时定量聚合酶链反应(RQ-PCR)、多色流式(MFC)等。MFC 通过分析细胞抗原表达情况区分正常细胞与异常细胞,具有快速、性价比高、覆盖范围广、灵敏度高、特异性高的特点。目前流式细胞术对急性髓系白血病(AML)检测敏感性为 10-3~10-4,虽然文献报道覆盖率为 80-95%,但是临床工作中低比例(低于 0.1%)MRD 检测、以及缺乏特异性标志的标本检测仍旧遇到瓶颈。以王卉主任、宫美维医师为代表的流式细胞室团队进行了一项研究,探讨 CD69 在急性髓系白血病(AML)微小残留病变(MRD)检测中的临床意义。
方法:采用多参数流式细胞术检测 40 例 AML(包括初治 AML 及治疗后 MRD)患者骨髓中 CD69 的表达率及表达强度,另选取 10 例 MRD 阴性的 AML 患者作为对照组。对照组患者经细胞形态学、流式细胞术、分子及遗传学检查证实其骨髓完全缓解状态。CD69 表达强度计算,采用每个患者同一管标本中 CD69 阴性的淋巴细胞作为校准参照,分别计算对照组正常髓系原始细胞和实验组恶性髓系幼稚细胞 CD69 中位荧光强度(MFI)与其 CD69 阴性淋巴细胞 CD69MFI 比值(MFIR)。
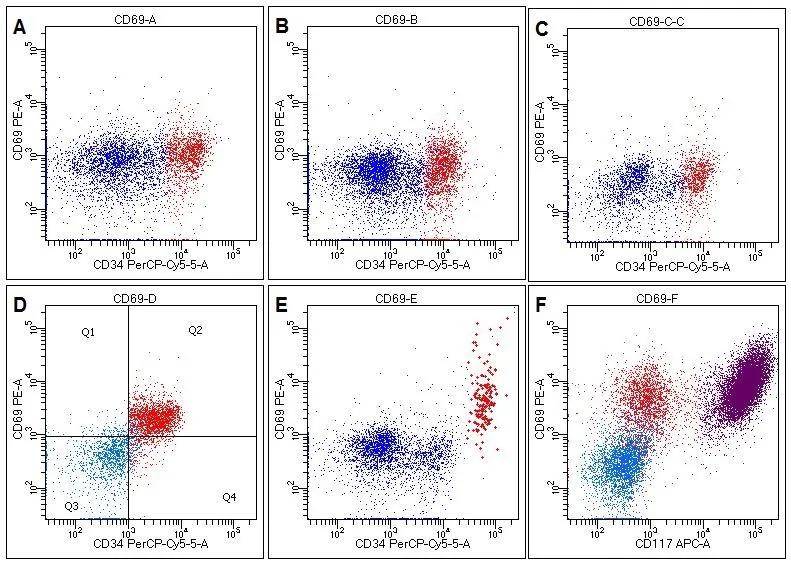
CD69 阴性和阳性的 MRD,红色细胞为肿瘤细胞
结果:CD69 在正常髓系原始细胞中不表达。在 40 例 AML 患者中,有 17 例(42.5%)CD69 表达阳性或部分阳性。阳性病例肿瘤细胞 MFIR 为 15.13+9.58,与对照组比较,具有显著性差异(P<0.01)。
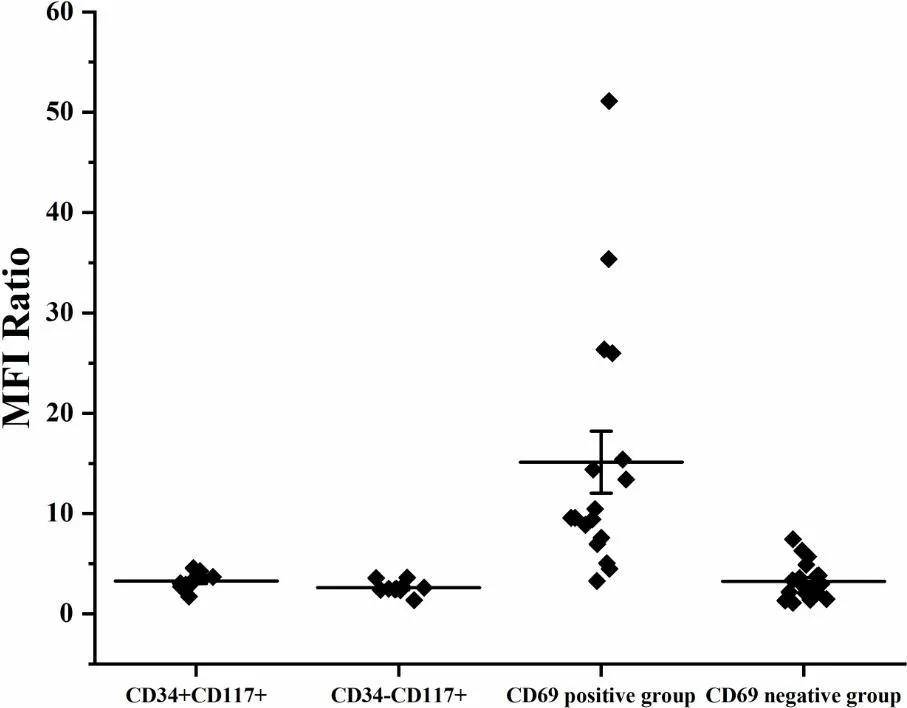
正常与恶性髓系原始细胞 CD69 中位荧光强度与 CD69 阴性淋巴细胞中位荧光强度比值(MFIR),CD34+CD117+、CD34-/CD117+组为正常髓系原始细胞组,CD69 阳性组和 CD69 阴性组为 AML 肿瘤细胞组,CD69 阳性组 MFIR 高于 CD69 阴性组和正常对照组(P<0.01),后两者无显著性差异
结论:CD69 可以作为一个新的 AML 特异性抗原加入 MRD 检测方案中,并有望成为嵌合抗原受体修饰的 T 细胞(CAR-T)治疗 AML 的一个新靶点。
简介

陆道培医疗集团流式细胞室宫美维医师,硕士研究生,助理研究员,中国中西医结合学会检验医学专业委员会流式细胞分析诊断专家委员会秘书。
三篇文章的通讯作者均为陆道培医疗集团检验科副主任、流式细胞室主任、信纳克实验室(CAP 认证实验室)主任王卉教授。
简介

陆道培医疗集团检验科副主任、流式细胞室主任、信纳克实验室主任(副院长级)。中国中西医结合学会检验专委会流式专委会主任委员;北京医学检验学会血液和体液检验分会副会长;中国非公立医疗机构协会血液委员会常委;中国临床流式联盟常委;中国抗癌协会淋巴瘤学组、中国血液免疫学会流式学组、中国生物工程学会细胞分析专委会、北京细胞生物学会等诸多学会常委、委员和特聘专家。从事流式临床诊断 19 年,独立签发 30 余万份报告;全国 28 个省(包括台湾)讲座 600 多场,为全国 26 个省(包括台湾)百家三甲医院培训了进修医。
科研创新,竞胜之道。陆道培医疗集团作为目前国内最大的造血干细胞移植中心,拥有专业的病理和检验医学团队,各实验室之间紧密协作,及时为临床一线医生提供精准的检验报告,为患者的正确诊断和治疗争取宝贵的时间,其检验报告的准确性和易读性得到业内的广泛认可。
