2018临床研究及生物样本分析(北京)
峰会举办时间:2018年10月25~27日
举办地点:中国 北京云瑧金陵莲花酒店(世纪莲花酒店)
主办单位:北京医药行业协会
中华全国工商业联合会医药业商会
承办单位:北京阳光德美医药科技有限公司
北京阳光诺和药物研究有限公司
顾问机构:北京医院
中日友好医院
首都医科大学附属北京同仁医院
天津医科大学肿瘤医院
北京协和医院
北京大学第三医院
中国人民解放军总医院(301医院)
江苏省人民医院
首都医科大学附属北京世纪坛医院
北京大学临床药理研究所
中国人民解放军307医院
中国人民解放军东部战区总医院
2018临床研究及生物样本分析(北京)峰会,由中华全国工商业联合会医药业商会与北京医药行业协会联合主办,于2018年10月25~27日在北京云瑧金陵莲花酒店举行,大会围绕中国创新药的研发现状、审评及核查政策与要求;仿制药一致性评价中临床设计的难点药物以及生物样本分析的科学性及合规性进行相关议题的分享与交流。
本届大会旨在促进中国创新药的临床医学设计实施技术原则的交流,结合政策法规,进行临床研究探讨,为正在研发申报中的创新药物提供交流的平台。大会组织的活动有:带领参会者进行生物样本检测项目的现场核查模拟、及常见问题的探讨;与全国 I 期基地主任及研究人员,就基地现状进行相关交流活动。大会举办期间将组织仿创药审评及政策研讨、创新药临床研讨、仿制药临床研讨、生物样本检测研讨等主题论坛等活动。
会议日程
1会前签到(10月25日,沙龙日)
· 签到:8:00~24:00 北京云瑧金陵莲花酒店
· 15:00~19:00 :生物分析实验室核查培训沙龙(金伟凯科技园 - 阳光德美实验室
检测项目的核查模拟、常见问题探讨。
2第一天上午(10月26日,会议日)
· 政策研读专场-第一日上午专场
· 08:20 北京医药行业协会领导致开幕词
· 08:30 中华全国工商业联合会医药业商会领导致开幕词
主持人:北京医药行业协会领导、中华全国工商业联合会医药业商会领导
· 08:40 基于新形势下的临床研究现场核查政策和要求解读
李见明 CFDI 领导、专家
· 09:20 新药和仿制药申报的注册法规及进度情况解读
胡美芳 北京市食品药品监督管理局 药品注册处处长
· 10:00 基于ICH新形势下新药研发和仿制药一致性评价的政策解读
高晨燕 CDE生物制品临床部部长
· 10:40 仿制药资料审查问题解析
张学辉 CDE统计与临床药理学部审评员
· 11:20 基于医药行业和新药研发/仿制药评价或医药产业政策的分析和分享
北京医药行业协会领导、专家
· 12:00 午餐及休息
3第一天下午(10月26日,会议日)
· 创新药临床研讨专场-第一日下午专场
· 13:00 基于核医学的肿瘤药物前期临床研究的思路探讨
江骥 北京协和医院 临床药理和核医学专家
· 13:40 肿瘤药物0期临床研究的思路和案例分析
王兴河 北京世纪坛医院I期主任
· 14:20 真实世界的肿瘤研究
吴一龙 中山大学肿瘤科主任兼副院长(待定)
· 15:00 茶歇与交流时间
· 15:15 传统与小分子靶向抗肿瘤药物的临床研究策略探讨及案例分析
刘泽源 307医院核查专家
· 15:55 临床试验设计的统计学考虑
刘玉秀 中国人民解放军东部战区总医院 CDE审评咨询专家
· 16:35 创新药及体内高疑难检测药物的方法开发及案例分享
郝光涛 北京阳光德美医药科技有限公司 副总经理
4第一天下午(10月26日,会后沙龙)
· 活动:阳光德美-I期基地小型研讨会(18:00~20:00 金伟凯科技园多功能厅)
· 与全国I期基地主任及研究人员,就基地现状进行相关交流并开展相关议题研讨,会后提供自助晚餐。
5第二天上午(10月27日,会议日)
· 创新药临床研讨专场-第二天上午专场①
· 08:30 新形势下创新药中美双报TQT研究思路和探讨
李海燕 北医三院机构主任/心内科专家
· 09:10 创新药I期临床试验设计思路及物料平衡研究的浅析
邵凤 江苏省人民医院I期临床基地主任
· 09:50 基于II/III期服务的新形势下非肿瘤药物创新药I期临床研究思路
史爱欣 北京医院I期临床基地主任
· 10:30 创新药临床研究中AE解读和研究提示
王进 北京世纪坛医院I期教授
· 11:10 抗肿瘤药物临床研究设计和思路
史业辉 天津肿瘤医院I期病房主任(待定)
· 仿制药临床研讨专场-第二天上午专场②
· 08:30 仿制药评价的基于统计学样本量估算思路和案例分享
魏敏吉 北大药理所 药代专家
· 09:10 仿制药临床现场核查要点及案例分享
赵秀丽 北京同仁医院I期基地主任、现核查专家
· 09:50 高变异仿制药BE设计思路和经典案例分享
王睿 301医院l期基地主任
· 10:30 内源性仿制药BE设计思路和经典案例分享
曲恒燕 307医院I期临床研究室主任
· 11:10 预试验结果对正式试验提示的经典案例分享
郝光涛 北京阳光德美医药科技有限公司 副总经理
· 12:00 午餐及休息
6第二天下午(10月27日,会议日)
· 生物样本检测专场-第二日下午专场
· 13:00 CFDA生物样本分析指导原则的历史和现状
李劲彤 中日友好医院药物临床试验研究中心副研究员
· 13:40 新形势下生物分析实验室的稽查核查要点
陈学义 北京阳光德美医药科技有限公司
· 14:20 FDA、CFDA对生物分析实验室的质量体系的规范化要求
举晓霞 北京阳光德美医药科技有限公司
· 15:00 茶歇与交流时间
· 15:15 大分子生物样本分析案例分享
余丽英 北京阳光德美医药科技有限公司
· 15:55 FDA、CFDA对数据溯源相关的生物分析电子数据的采集、备份、安全及电子签名的法规要求
陈飞 北京阳光德美医药科技有限公司
· 16:35 FDA、CFDA对生物样本分析计算机化系统验证的法规要求
周壮 北京卓亚医药科技有限公司
· 17:15 主持人致闭幕词
7关于德美 中美双报生物样本检测平台
北京阳光德美医药科技有限公司是专注于中美双报的大型生物样本检测平台,注册资金2000万,检测实验室总计一千多平米,总投资超过4000万,拥有世界顶级生物样本分析测试仪及软硬件配置,完善的SOP体系。德美团队以其强大的方法开发能力、高效快速合规的项目实施能力,全力推动和保障客户国内及国际研究项目的申报成功。
会议报名
本次大会收取会议费(含会议资料和茶歇),交通及住宿费用自理;9月25日前缴费的代表享有优惠,3人及以上同单位代表可享受团购价格优惠;报名截止日期10月20日。
注册类别 | 个人(9月25日前) | 3人及以上团 | 现场缴费 |
| 费用 | 900元 | 800元 | 1200元 |
1. 缴费方式
A. 银行转账汇款:
开户名:北京千帆国际展览服务有限公司
开户银行:中国工商银行股份有限公司北京东城支行
账 号:0200080709024732269
B. 现场缴费:支票、现金支付,不支持任何形式的刷卡缴费。
C. 北京医药行业协会:向协会报名,会员报名享会员价。
D. 中华全国工商业联合会医药业商会:向商会报名,会员报名享会员价。
2. 备注
1) 请参会者务必于2018年10月10日之前,填写报名回执,上传付款凭据,并发送至邮箱huangcx@bjscinovo.com。组委会保留由于不可控因素导致的发言人更换和议程时间调整的权利。
2) 汇款请注明“2018临床研究及生物样本分析(北京)峰会报名”和参会人姓名(如为主办方会员,请注明主办方名称)、发票抬头单位名称。如无法添加附言,请务必通过电子邮件告知会务组,以便确认款项归属。
3) 提前注册的参会代表将于会议当天在现场拿到发票,现场缴费的代表将于会后由主办方以快递的形式邮寄发票(到付)。
4) 本次会议出具增值税普通发票,发票科目为会务费。
>> 联系我们 <<
联系人: 黄老师:13366755157,huangcx@bjscinovo.com
联系人: 赵老师:15710073691 ,hbz@bjscinovo.com
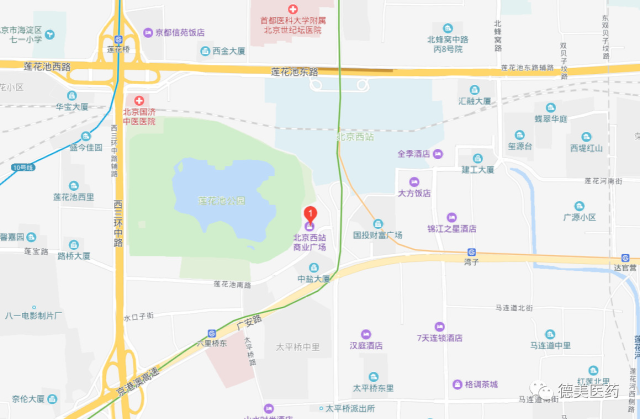
>> 酒店地址 <<
酒店地址:北京市莲花池南路1号 联系电话:010-53256699