2019 年 5 月 31 日 ~ 6 月 4 日,一年一度的美国临床肿瘤学会(American Society of Clinical Oncology,ASCO)年会在芝加哥召开,南京鼓楼医院泌尿外科青年医生张顺受郭宏骞教授委派参与此次盛会。
ASCO 成立于 1964 年,是全球规模最大、最具影响力的肿瘤专业学术组织,致力于肿瘤的预防、治疗及患者生活质量的改善。其会员覆盖全球 100 多个国家,包括来自肿瘤学及相关领域的 40000 多名医疗护理专家。每年六月初,ASCO 年会均在美国中部城市芝加哥举行,探讨肿瘤学领域的最新进展。本届参会人数超过 40000 名,共有 2450 多篇会议报道和壁报交流,另外有 2500 多篇摘要在线发布。
ASCO 内容主要分布在消化、呼吸、血液等肿瘤领域,泌尿系肿瘤所占比例相对较小。除了大家最常关心的 OS、PFS 等,大会同样会花精力去关注和聚焦患者的生存质量、不良反应等。本次大会的主题「Caring for Every Patient, Learning from Every Patient(关心每一位患者,向每位患者学习)」也突出了这一点。限于医疗环境和医患供需的严重失衡,国内的医务工作者往往会忽略这些。让我们怀着对生命的尊重:To Cure Sometimes,To Relieve Often,To Comfort Always。
会议于当地时间 5 月 31 日下午开始,首日日程泌尿外科方面仅涉及到前列腺癌领域。下面,就让我们来看看有哪些精彩内容吧!

TITAN 研究:结果喜人
Apalutamide 是抗雄激素药物,可强效抑制 AR 活化、核转位、与共激活因子的结合和 AR 介导的基因表达。
TITAN 研究旨在确定 ADT 联合 APA(Apalutamide)能否更有效地改善 mCSPC 受试者的总生存期(OS)或影像学无进展生存期(rPFS)。
方法:在这项随机、双盲、安慰剂对照的 3 期研究中,将 mCSPC 受试者按 Gleason 评分、既往多西他赛的使用情况和地区等进行分层,然后随机分配(1:1)至 APA(240 mg / d)或安慰剂组(PBO)。所有患者都接受了持续的 ADT。主要终点是 rPFS 和 OS。首次计划的 OS 中期分析发生在约 50% 的预期事件之后。
结果:525 例患者随机分配至 APA,527 例随机分配至 PBO。基线情况:中位年龄为 68 岁; 8% 的患者有过局部治疗; 11% 使用过多西紫杉醇;63% 为高瘤负荷,37% 为低瘤负荷。中位随访时间为 22.6 个月,66% 的 APA 和 46% 的 PBO 患者仍在接受治疗。APA 显著改善 rPFS(HR,0.48; 95%CI,0.39 - 0.60; p <0.0001),死亡或放射学进展风险降低了 52%,且在所有分析的亚组中均观察到了获益。PBO 组中位 rPFS 为 22.1 mos,APA 组尚未达到。
APA 的 OS 也显著改善(HR,0.67; 95%CI,0.51 ~ 0.89; p = 0.0053),死亡风险降低了 33%。两组均未达到中位 OS。
APA 组的化疗开始时间也显著延迟(HR,0.39; 95%CI,0.27 ~ 0.56; p <0.0001)。3 或 4 级不良事件(AEs)(42%APA,41%PBO)的发生率相似,由 AE 引起的停药率(8%APA,5%PBO)较低。结论:mCSPC 的患者,包括高瘤负荷、低瘤负荷以及之前使用过多西紫杉醇患者,使用 ADT 联合 APA 可以显著改善 rPFS 和 OS,其安全性是可接受的。
本次研究结果也同步发表在 The New England Journal of Medicine 。
对参与其中研究的小编来说,能在大会现场听到如此出色的研究结果,内心还是很激动的。
在美国,Apalutamide 于 2018 年 2 月获批,用于治疗存在高转移风险的非转移性去势抵抗性前列腺癌(nmCRPC)患者。此次批准,使 Apalutamide 成为全球首个治疗 nmCRPC 的药物。在欧盟,Apalutamide 于 2019 年 1 月获批相同的适应症。
国家药品监督管理局药品审评中心于 5 月 29 日正式公布了 Apalutamide 等 26 个无异议的品种作为第二批临床急需境外新药品种。Apalutamide 本次因在非转移性去势抵抗性前列腺癌(NMCRPC)中临床优势明显,获得 CDE 的认可。按照相关规定,Apalutamide 被列入临床急需境外新药名单,可直接提出上市申请,CDE 建立专门通道并在 6 个月内完成技术审评。
距离国内上一个前列腺癌药物治疗的「利器」—— ZYTIGA上市已经过去了四年。令人欣慰的是,最快今年年底,Apalutamide 的上市将会让泌尿科和肿瘤科医生又多一个强有力的抗癌武器,而广大患者也会多一份选择和希望。
Alliance A031201 研究:出乎意料
本研究是对比恩杂鲁胺与恩杂鲁胺+abiraterone 和泼尼松治疗转移性去势抵抗性前列腺癌(mCRPC)的 III 期临床试验
方法:根据 PCWG 2 标准证实存在进展,排除既往使用过恩杂鲁胺或abiraterone 治疗或在 mCRPC 使用紫杉烷的患者,然后按 1:1 随机分配至恩杂鲁胺或恩杂鲁胺+abiraterone ,保持 ADT 治疗。主要终点是 OS,次要终点包括 rPFS 和治疗 PSA 下降。
Apalutamide 2014 年 1 月至 2016 年 8 月期间,恩杂鲁胺组为 657 名,恩杂鲁胺+abiraterone 组为 654 名。15.6% 的患者为高风险,35.3% 为中度风险,48.1% 为低风险。中位 OS 分别为 33.6 mo(95%CI 30.5 ~ 36.4)和 32.7 mo(29.9 ~ 35.4),p = 0.53。50% 的 PSA 下降率为 80% 和 76.5%。
3 ~ 5 级不良事件分别为 55.6% 和 68.8%。由于不良事件引起的治疗中断发生率分别为 5% 和 12%,退出率分别为 5% 和 13%,进展或死亡率分别为 57% 和 48%。
结论:ZYTIGA加入恩杂鲁胺不会延长 mCRPC 患者的生存期。该组合比单用恩杂鲁胺产生更多的 AE。
在今年 ASCO-GU 我们报道了来自意大利圣基亚拉医院的 Orazio Caffo 教授 CHEIRON 研究的初步结果。它是恩杂鲁胺联合多西他赛治疗 mCRPC 的Ⅱ期随机临床研究,初步结果显示恩杂鲁胺联合多西他赛较单用多西他赛显著改善疾病控制率,但同样不能提高 OS。
随着药物选择越来越多,大家都在不断尝试联合治疗以期更好的治疗效果。目前几项恩杂鲁胺联合abiraterone 或多西他赛治疗 mCRPC 临床试验的初步结果都提示不能显著延长 OS。随着越来越多临床研究的关注,也许在亚组分析的特定人群中能取得「意料之中」的结果。
TOPARP-B 研究:靶向时代已经来临
Olaparib(奥拉帕尼)是多聚腺苷二磷酸核糖聚合酶 (PARP) 的抑制剂。目前已被批准用于治疗 BRCA 基因突变的卵巢癌。这种药物被认为对于 DNA 修复相关基因缺陷引起的癌症有着良好作用。
既往 TOPARP-A 的单臂临床研究结果,证实了奥拉帕尼在经化疗后多线治疗的转移性 CRPC 患者(尤其是有 DNA 修复缺陷患者)的初步疗效和安全性。
TOPARP-B 试验:奥拉帕尼治疗转移性去势抵抗前列腺癌携带 DNA 损伤修复缺陷患者的 2 期随机试验研究方法:对紫杉醇化疗 ≥ 1 次后 mCRPC 进展的任何 DDR 基因的改变的患者以 1:1 随机分配至 400 mg 或 300 mg 奥拉帕尼 BID,旨在排除任一组中 ≤ 30% 的缓解率(RR)。主要终点 RR 定义为放射学缓解(RECIST 1.1)和/或 PSA50% 下降和/或循环肿瘤细胞(CTC)计数转换(Cellsearch 系统;≥ 5 至<5),4 周后确认。次要终点包括无进展生存期(PFS),耐受性。研究结果:92 名患者接受治疗且主要终点可评估(70 名 RECIST 可评估;89 名 PSA50% 可评估;55 名 CTC 可评估)。所有患者在 ADT 后疾病进展; 99% 为多西他赛后,90% 为abiraterone /恩杂鲁胺,38% 为卡巴他赛后。
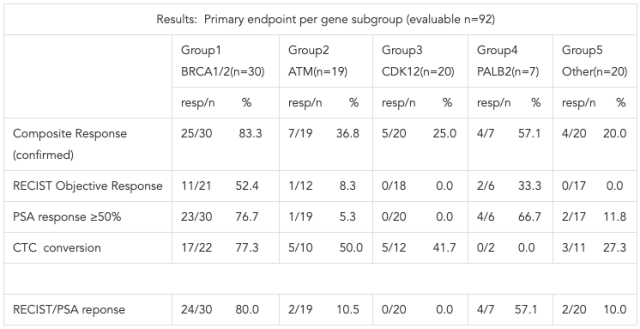
研究结论:奥拉帕尼对存在 DDR 基因缺陷的 mCRPC 具有很强的抗肿瘤活性,对 BRCA1 / 2 异常肿瘤最敏感。400 mg 组中的总 RR 为 54%(95%CI 39%~69%,达到主要终点的阈值),300 mg 组中总 RR 为 37%(95%CI 23%~53%)。中位随访时间为 17.6 个月,整体中位 PFS(mPFS)为 5.4 个月。亚组分析表明,每个基因突变的应答率为:BRCA1 / 2 80%(24 / 30;mPFS 8.1 个月); PALB2 57%(4 / 7;mPFS 5.3 个月); ATM 37%(7 / 19;mPFS 6.1 个月); CDK12 25%(5 / 20;mPFS 2.9 个月); 其他 [ATRX,CHEK1,CHEK2,FANCA,FANCF,FANCG,FANCI,FANCM,RAD50,WRN] 20%(4 / 20;mPFS 2.8 个月)。在 BRCA1 / 2(22 / 30; 73%)和 PALB2(4 / 6;67%)亚组中观察到最高的 PSA50% 应答率。
尽管 mCRPC 的治疗有了一些令人瞩目的进展,但是迄今为止仍没有针对前列腺癌不同分子亚型的特异性治疗运用于临床。奥拉帕尼的出现或许可以使前列腺癌在精准药物治疗的道路上迈出具有现实意义的一步。小编觉得「何时」进行前列腺癌基因检测会在不久的将来取代「是否」进行基因检测成为大家讨论的话题。
TAXOMET 研究:二甲双胍的跨界之旅
二甲双胍是应用广泛的降糖药,除了降血糖的作用,还被逐步发现在抗衰老、抗肿瘤等方面作用。一些回顾性队列研究表明,二甲双胍可降低前列腺癌发生率和死亡率,添加二甲双胍可以增强 mCRPC 患者的多西他赛化疗的疗效。那二甲双胍的泌尿跨界之旅顺利吗?
一项前瞻性多中心随机对照Ⅱ期研究 TAXOMET,比较多西他赛联合二甲双胍与多西他赛联合安慰剂治疗转移性去势抵抗前列腺癌(mCRPC),主要研究终点为 PFS 反应率(≥ 50% 降低),次要研究终点包括客观缓解率(ORR)、PFS、OS、毒性和生活质量(QoL)。研究共纳入 99 例患者,二甲双胍联合组和对照组没有观察到区别,其中 PSA 反应率两组均为 72%,ORR 均为 28%,临床或生物学中位 PFS,两组分别为 7.3 个月和 5.8 个月,p = 0.848,中位 OS 两组分别 24.2 个月和 19.7 个月(p = 0.53)。不良事件方面,除了二甲双胍组有腹泻更常见的趋势(70% 和 50%,p = 0.072;3~4 级事件较少)外,其余两组之间没有差异。根据治疗期间两组之间的 QLQ-C30 评分,QoL 没有差异。TAXOMET 研究表明,二甲双胍的添加并未给患者带来任何获益。
尽管二甲双胍在本研究遭遇滑铁卢,但在本次大会的其他肿瘤领域也会有相应研究结果出炉,希望能听到胜利的声音。我们往往期望用一个副作用较小的药物来增强现有的疗效,比如度他雄胺联合abiraterone 治疗前列腺癌等。尽管道路是曲折的,但我们坚信前途是光明的。
EORTC 1333 / PEACE III 研究:多多益善
Ra223 是镭的同位素,通过发射高能α射线,促使骨转移部位的肿瘤细胞双链 DNA 发生断裂,其射程仅为 2 ~ 10 个细胞长度,可减少对周围正常组织的损害。目前被 FDA 批准用于治疗合并骨转移但无其他内脏转移的去势抵抗性前列腺癌。EORTC 1333 / PEACE III 研究比较的是恩杂鲁胺联合 Ra223 氯化镭与单用恩杂鲁胺在应用骨保护剂后的骨折率。
既往 ERA223 研究显示abiraterone 与 Ra223 氯联合治疗后骨折率显着增加。因此,FDA 和 EMA 建议不要使用这种组合。应用骨保护剂(唑来膦酸、地诺单抗等)能否减轻骨折风险,并且恩杂鲁胺 +氯化镭组合中是否存在这种风险目前尚不清楚。EORTC 1333 / PEACE III 研究显示显示无症状 mCRPC 中恩杂鲁胺的骨折风险为 13%,与既往的报道一致。当将 Ra223 加入到恩杂鲁胺中时,这种风险显着增加至 33%。引人注目的是,在首次注射 Ra223 前至少 6 周开始强制性连续给予骨保护剂几乎可以消除风险,这强调了治疗 mCRPC 患者骨保护剂应用的重要性。
小编在临床中对于 mCRPC 患者常规应用双磷酸盐类等骨保护剂。双磷酸盐类药物的主要作用机制是阻挡破骨细胞对骨的破坏溶解和抑制破骨细胞的活性,应用时需要注意肾功能损害、颌面骨坏死等不良反应。
ARAMIS 研究:关注生活质量和疼痛
Darolutamide 是具有独特化学结构的非甾体雄激素受体拮抗剂,其分子构象与 Enzalutamide 及 Apalutamide 不同,与 AR 受体具有高亲和力,具有较强的拮抗作用,可抑制前列腺癌细胞的受体功能和生长。
ARAMIS 研究探索的是 Darolutamide 对患有非转移性去势抵抗性前列腺癌(nmCRPC)的患者的疼痛和生活质量(QoL)的影响。在今年 ASCO-GU 上我们也做过相关报道。研究显示:Darolutamide 较安慰剂组显著延长患者无转移生存期,明显改善疼痛进展时间和生存质量(QoL)。试验中 Darolutamide 的不良反应(如高血压、癫痫发作、精神损害、骨折等)同安慰剂组无明显差异,展现出良好的安全性。
GETUG-AFU 16: 五年后再来
本研究是一项来自法国的前瞻性、多中心、随机对照 3 期临床研究,对挽救性放疗联合短期内分泌治疗和单纯挽救性放疗进行比较。
研究方法:T2、T3 或 T4a 的接受过根治性手术的前列腺癌患者;根治性手术后至少 6 个月 PSA 保持在 0.1 ng/ml,之后出现升高(0.2 ~ 2 ng/ml);没有临床病灶的证据;未接受内分泌治疗或放疗。患者随机分配至标准挽救性放疗组(RT 组)或放疗联合短期内分泌治疗组(RT+HT 组,因此内分泌治疗时间为 6 个月)。主要研究终点为无进展生存。
2016 年在 Lancet Oncol. 首次报告了随访 5.3 年的 PFS 数据(RT+HT vs. RT:80% vs. 62%;p< 0.0001)。而本次大会,研究者带来了最新的数据。截止 2019 年 3 月,平均随访时间为 112 个月。无论低风险组还是高风险组,RT+HT 组均显著延长 PFS(HR = 0.54,CI95% 0.43 ~ 0.68,p<0.0001)。RT 组和 RT+HT 组的 10 年 MFS 率分别为 69%(CI95% 63 ~ 74)和 75%(CI95% 70 ~ 80)。
此次随访 9 年的数据显示,挽救放疗联合短期放疗可显著改善患者 10 年无转移生存率,证实了该策略可被视为根治性前列腺切除术后挽救治疗的新标准。本项目研究者称,未来 5 年、10 年会再次向大家汇报后续随访。
小编和同行的几位教授均不禁感慨,随着医学发展,前列腺癌患者的生存期越来越长,越早发现治疗效果越好。
继续教育
今天的 Education Session(继续教育)部分是关于 PSMA 在前列腺癌诊断和治疗方面的进展。Education Session 内容主要是展示本年度各个瘤种最重要、最热门的话题,目的是向参会人员传递最近的临床研究进展信息。
我科对 PSMA 的研究和应用也做了大量工作,陈梦霞博士、张成伟博士在今年五月的 AUA 2019 会议上进行了相关发言(点此查看)。目前,我科在 6 月 1 ~ 2 日举行的「第一届中德前列腺癌诊疗论坛」也对 PSMA 的研究与应用进行了热烈的讨论,欢迎大家关注。
小编日常负责科室 30 余项药物临床试验,对相关培训也是很感兴趣。正好发现有个讲座:How to Initiate and Integrate Clinical Trials Into Your Practice。听下来以后感慨,临床试验责任重大,而其中临床研究者是最容易犯错误的,也是政府监管的重点。
好的临床试验项目质量来源于不断的学习和改进。从自我检查,内部监督和外部核查三方面质控,才能实现 GCP 的要求。