当地时间 6 月 1 日上午 9:30,ASCO 2019 开幕式正式开始,宏大的主会场容纳近万名听众。ASCO 主席 Monica M. Bertagnolli 用一张张图片生动的讲述她在美国各州社区医院的经历,阐述了本次大会的主题「Caring for Every Patient, Learning from Every Patient」。之后出场是一名激情四射的新西兰小伙 Edmond Ang,他是一名肿瘤学医生。在整个演讲中,他反复强调一个词「PEOPLE」。他说:肿瘤学说到底就是人关心照顾人,但是现在来自工作的生理、心理、情绪等压力会影响到我们,改变了这个初衷。他用自己的故事深深打动了在场的每一位。小编觉得相较于国人的含蓄内敛,很多外国友人更擅长去表达自己的情感,而我们身边也有很多有温情、有责任、也有希望的医患故事,最近的医疗人文纪录片《医心》在热播,也希望有更多人来传递你我身边的故事。
现场有个很有意思的 M0 CRPC 相关的病例讨论,讲述的是「W」两兄弟倔强而坎坷的前列腺癌治疗经历。下文将会有一些投票和资料复习,来引导大家参与和讨论。
首先,回顾一下 M0 CRPC 的定义:睾酮处于去势水平,同时影像学评估未发现远处转移病灶。既往传统的影像学评估手段主要包括胸腹 CT 及骨扫描,但目前 PET/CT 在发现较小的转移灶方面有着显著优势,尤其是近年来研究火热的 PSMA PET/CT。
病例 1:
EW,65 岁,既往健康状况可,虔诚的教徒,家族史:兄弟 TW 在 60 岁时确诊前列腺癌。EW 治疗前 PSA 22ng/mL,临床分期 T3N0M0,Gleason 评分 4+4 = 8 份,穿刺 9/12 阳性,骨扫描和 CT 提示无转移。
老大爷比较有主见,拿到病理结果后去了好多家医院,看了很多门诊,把泌尿外科、放疗科、肿瘤科的专家都看了个遍,最后做出了决定:拒绝参加临床试验和手术,选择放疗!
投票环节:对于这种高危的前列腺癌患者的治疗是什么?
A. ADT
B. 放疗+Abiraterone+ADT
C. 放疗 +ADT
D. 放疗+多西他赛化疗+ADT
——现场专家 73% 选择了 C. 放疗 +ADT
2014 年,一项纳入 27 项 RCT 研究的 meta 分析发现:对于局限性前列腺癌,外放疗联合 ADT 的总生存率、肿瘤特异性生存率和无生化复发率显著高于单纯外放疗。此外,与 EBRT 联合短期 ADT(<10 个月)治疗相比,EBRT 联合长期 ADT 治疗的总生存率、肿瘤特异性生存率和无生化复发率更高。
NCCN 目前推荐对于局限高危性前列腺癌,采用外放疗(EBRT)+长程 ADT(1.5~3y)治疗。
EW 老大爷治疗后效果不错,可是在 36 个月后生化复发了:PSA 5.7ng/mL,倍增时间>12 个月,常规的骨扫描和 CT 提示无转移。老大爷又晃了一大圈,听了各个学科专家的意见后,自我思索半天,觉得吃什么药啊,祷告一下就够了, Wish God bless me。
投票环节:在这种情况下,再次启动 ADT 时机的主要依据是什么?
A. 单纯 PSA 升高
B. PSA 倍增时间
C. 有新的影像学证据
D. 等至 M1(骨扫/CT 检出)再治疗
——72% 专家选择了 B. PSA 增长变化
PSA 倍增时间(PSADT)是通过血清 PSA 动力学研究得到的监测指标,可用于评估前列腺癌疾病进展。既往的一项研究显示:倍增时间<3 个月,中位至发生转移时间约为 9 个月。倍增时间为 9~14.9 个月,中位至发生转移时间为 40 个月。
前列腺癌根治术后患者,如 Gleason 评分 5~7 分,2 年后生化复发,PSADT>10 个月相比于 PSADT ≤ 10 个月的 5 年的无转移进展率由 92% 降低至 34%。
由此可见,PSADT 在预测前列腺癌根治术后临床复发、放疗后临床进展、前列腺癌带瘤生存时间和特异死亡率及监测观察等待治疗方面都有重要价值。
EW 老大爷现在的 PSADT<8 个月,PSA 12.7 ng/mL。后面怎么办呢?
投票环节:目前在倍增时间<10 个月情况下,治疗方案是什么?
A. 持续 ADT
B. 间断 ADT
C. ADT+Abiraterone
D. 继续观察直至 M1(骨扫描+CT 检出)
——44% 的专家选择 A. 继续 ADT,33% 的专家选择 C. ADT+Abiraterone
在一项随机对照 ADT+Abiraterone 和单用 ADT 治疗生化复发的未接受过内分泌治疗的无转移的前列腺癌研究中显示:主要终点 PSA 无复发生存期为 28.3 vs 21.1 个月(P = 0.007),两者还是有显著差异的。那么 PSA 无复发生存期与 MFS、OS、QoL 有相关性吗?这个问题值得未来继续探索以解答我们的疑惑。
老大爷在医生的劝说下终于开始 ADT 治疗了,PSA 反应很好都测不出来并且维持了 12 个月。但是好景不长, PSA 又开始慢慢上升>2ng/mL,倍增时间<10 个月,常规的骨扫描和 CT 还是提示无转移。倔强有信仰的老大爷依然坚持只打针(ADT)+ 祷告,拒绝其他治疗方案。EW 大爷的随访到此结束了。
投票环节:伴随 PSA 上升的 M0CRPC 在 2019 年还存在吗?
A. 存在 B. 不存在
——69% 专家认为还依然存在,31% 认为在 PSMA PET 等应用下,是不存在 M0 这个状态的。
点评专家认为 CRPC 阶段的 M0 是 M1 的一种特殊形式。M0 是通过传统常规的骨扫描和 CT 来判断的,而其中大部分通过包括 PSMA PET 、DW-MRI 等新型影像技术能够发现转移。M0 具有根据不同的倍增时间表现出不同的特征,PSADT 较短则表现出很高的侵袭性,反之则进展缓慢惰性强。
病例 2:
聊完 EW,下面再说说他的兄弟 TW。
TW,平素体健,无其他伴随疾病。60 岁时行前列腺癌根治术,术后因 PSA 残留行挽救性放疗,未予 ADT。后因 PSA 升高加用 ADT,PSA 下降明显至检测不出来。随后 PSA 再次上升,倍增时间<6 个月,常规骨扫描和 CT 未见转移。
TW 符合多项临床试验入组标准,但是因为最近在拉斯维加斯赚了一笔大钱,老大爷有钱任性,愿意自掏腰包支付任何治疗,就是不接受临床试验,他觉得不靠谱。(PS:老大爷的想法是不对的,美国国立综合癌症网络 NCCN 认为所有癌症患者的最佳治疗都在临床试验中,并且特别鼓励患者们参加临床试验。这段话在各个癌种指南中写在几乎每一页的底部,也是在不断提醒我们临床医生!)
投票环节:TW 这时候最佳治疗选择是什么呢?
A. Abiraterone+泼尼松
B. 阿帕鲁胺
C. 继续 ADT 直至出现明显进展
D. Darolutamide
E. 恩杂鲁胺
——46% 专家选择了 B. 阿帕鲁胺
对于 M0CRPC,FDA 已经批准两种药物阿帕鲁胺和恩杂鲁胺,加上已经有临床试验结果的 Darolutamide。那么现在我们来对比下,首先它们都是靶向雄激素受体(AR),阻断肿瘤细胞内 AR 的信号通路。阿帕鲁胺和恩杂鲁胺分子构象类似,而 Darolutamide 分子构象与前两者都不同。
那么到底哪个效果更好呢?小编做了一个表格以便直观对比。因各项临床试验入组标准及研究方法略有差异,数据对比仅供参考。
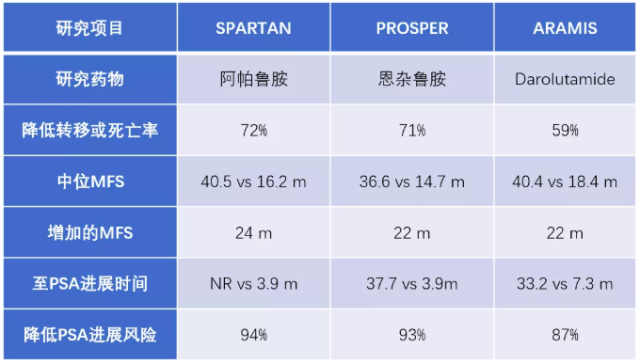
因死亡例数太少,无法比较 OS.
我想也是基于以上数据,大部分专家在 M0CRPC 阶段优先选择阿帕鲁胺。
最终 TW 选择了 yetanotherlutamide(代号),反应很好且 PSA 保持在 0.5ng/mL。两年半后 PSA 开始上升,倍增时间为 8 个月。常规的骨扫描和 CT 仍未见转移。
投票环节:这时候你会停用 yetanotherlutamide 吗?
A. Most Likely
B. Fairly Likely
C. Likely
D. Slightly Likely
E. Not Likely
——大多数专家选择了 E. Not Likely
在对 mCRPC 患者使用恩杂鲁胺治疗过程中,未发现影像学进展同时伴有 PSA 进展。在恩杂鲁胺组,从最低点到 MFS 时间一般比 PCWG2 要求到达 2ng/mL 的时间要短。在没有达到影像学进展之前,大多数患者都会有尚未达到 PCWG2 PSA 进展标准的 PSA 升高。但无论有无 PSA 进展,其侵袭性和影像学进展的类型都是相似的。
因此在应用阿帕鲁胺等雄激素受体抑制剂时候,对于仅有 PSA 进展的患者应再次评估确认,不轻易更换治疗方式。
TW 老大爷还是去了最好的州立医疗中心,做了 68 Ga-PSMA PET,发现 3 个骨转移灶。但是目前老大爷没有任何疼痛等症状。
投票环节:TW 这时候最佳治疗选择是什么呢?
A. Abiraterone+泼尼松
B. 继续阿帕鲁胺
C. 多西他赛化疗
D. 立体定向消融放疗 (stereotactic ablative radiotherapy, SABR)
E. sipuleucel
——31% 的专家选择了 B. 继续阿帕鲁胺
33% 的专家选择了 D. 立体定向消融放疗
TW 老大爷本次做了 68 Ga-PSMA PET,发现 3 个骨转移灶,但无法确认骨转移起始的时间点,因此建议 3 个月后复查 68 Ga-PSMA PET,如影像学进展,才认为考虑是否更换其他药物。当然在此期间,SABR 也是可以同时进行的。
最后总结下对于 M0CRPC 的患者治疗指导意见:
对于 PSADT ≤ 10 个月,建议阿帕鲁胺或恩杂鲁胺,且持续 ADT 治疗;
对于 PSADT>10 个月,可以观察且持续 ADT 治疗;
对于不希望或不能使用标准治疗且不愿意接受观察的高危转移进展患者,可选择 Abiraterone+泼尼松;
不推荐临床试验范围之外使用全身化疗或免疫治疗。
壁报分享:
一个壁报大厅可同时容纳数百份壁报展示,内容丰富多彩。那么多内容想在短时间内消化掉也是件痛苦并着快乐的事情。小编挑选了以下几份进行报道:
1. 新型 PARP 抑制剂 IMP4297 在中澳晚期实体瘤患者中的 I 期试验结果汇总分析
IMP4297 是一个具有独特化学结构和高活性潜能的新型 PARP1/2 抑制剂。动物实验数据表明,其抗肿瘤活性约为奥拉帕尼的 20 倍。在中国和澳大利亚同时开展了两项 I 期临床试验,评估 IMP4297 在晚期卵巢癌、乳腺癌,前列腺癌以及其他晚期实体瘤患者中的安全性、耐受性、药代动力学特征和抗肿瘤活性。
截至 2019 年 2 月 28 日,共有 58 例患者入组 2~100 mg 剂量组,其中 BRCA 突变患者 24 例。没有观察到剂量限制性毒性 (DLT)。在这两项临床试验中,比较常见的治疗相关不良事件 (TRAEs) 有白细胞减少 (22%),其次是贫血 (19%)、恶心 (16%) 和血小板减少 (16%)。大部分 TRAEs 为 1 级或 2 级,7 例患者发生 3 级及以上 TRAE (贫血 3 例;呕吐 1 例;血小板减少 2 例;AST 升高 1 例)。在 17 例有可测量病灶的 BRCA 突变患者中,客观缓解率为 41%,疾病控制率为 82%。
至 2019 年 2 月 28 日:5 mg 一例 BRCA 突变的 mCRPC 骨转移病人,用药 0.5 月 TPSA 降低 50%,用药 7 个月后调整至 20 mg,疾病稳定超过 13 个月,仍在给药。80 mg 一例 BRCA 突变的骨转移加脑转移的尿路上皮癌病人,用药 1.5 月后达到 PR,持续 PR 超过 6 个月,肿瘤缩小 76%,仍在给药。PARP 抑制剂能透过血脑屏障,作用于脑转移病灶,但是透过率不高。
IMP4297 一例在 BRCA 突变的尿路上皮癌的应用也给了小编一些想法,PARP 抑制剂在尿路上皮癌是否是继 FGFR 后又一个具有治疗前景的靶点,但是目前看来突变比例太低,想做一定数量研究还是有很多的困难。
IMP4297 具有良好的耐受性和明显的抗肿瘤活性。目前我科开展剂量扩展阶段 I 期临床研究,入组标准为至少一线治疗失败的晚期前列腺癌和尿路上皮癌 BRCA 突变患者。如有需要的患者可至南京鼓楼医院 1 号楼 18 层受试者接待室咨询。
2. 关注 ADT 的不良反应
一项前瞻性、随机试验中的心血管疾病发病率比较晚期前列腺癌患者的 GnRH 激动剂和拮抗剂。41 名患者随机分配至 GnRH 拮抗剂,39 名分配至 GnRH 激动剂。两组患者具有相似的年龄,基线心血管和前列腺癌特征。GnRH 激动剂组的 20%(n = 8)患者具有心脑血管事件,而拮抗剂的患者为 3%(n = 1)。使用 GnRH 拮抗剂在 12 个月时心脑血管试验的绝对风险降低为 18%(95%CI 5-31)。因此对于已有心血管疾病的患者来说,与 GnRH 激动剂相比,GnRH 拮抗剂心脑血管发生率更低。
目前我们临床中应用的大部分是 GnRH 激动剂,相信大多数泌尿外科医生没有多考虑心脑血管事件的问题。小编从事临床试验工作之前,很少注意过我们常规用药的副作用。比如比卡鲁胺这个基本的前列腺癌用药,之前没觉得有啥副作用。可是在临床试验中比卡鲁胺作为对照组,它所有的不良反应都要作为不良事件记录下来。这才慢慢发现患者有血尿、体重增加、胸痛、便秘等等,这些其实都是跟比卡鲁胺相关,只是我们平日不会去在意。但是对于晚期肿瘤患者来说,对于任何药物反应他们内心还是比较在意和紧张的,如果是比较细腻内向的患者,甚至还会焦虑。
因此在临床中,小编会详细交代下治疗的常见的不良反应,让患者提前有所了解放宽心,这样患者也不会总是咨询你,实现双赢的局面。同时这也是对大会主题「Caring for Every Patient, Learning from Every Patient」的实践。
3. 关注 Abiraterone 进展后,恩杂鲁胺的联合治疗
恩杂鲁胺与 LY3023414 或安慰剂(PL)在 Abiraterone 进展后 mCRPC 患者中疗效的 1b / 2 期研究。LY3023414 是一个新型的 PI3K/mTOR 抑制剂(类似于依维莫司)。临床前和 1 阶段结果表明 PI3K / mTOR 途径抑制可以增强雄激素受体抑制。中位数 PCWG2-PFS 为 3.7mos(LY + ENZ)vs 2.9 mos(PL + ENZ)(HR 0.66,95%CI 0.43,0.99; p= 0.0208)。结论:恩杂鲁胺+ LY3023414 联合治疗具有临床可控的安全性。PCWG2-PFS 的主要终点已经达到,并得到 AR-V7 阴性患者中 rPFS 延长的支持。
恩杂鲁胺与 Pembrolizumab 在 Abiraterone 进展后 mCRPC 患者中疗效的 1b / 2 期研究。Pembrolizumab 是 PD-1 抑制剂,目前国内已经上市,中文名帕博利珠单抗,商品名可瑞达。目前国内适应症黑色素瘤和 NSCLC。本研究中治疗相关的 AE 发生在 63 例(91%)患者; 最常见的(≥ 20%)是疲劳(30%),皮疹(23%)和恶心(22%)。 3/4 级治疗相关的 AE 发生在 28 例(41%)患者中; 最常见的是皮疹(10%)。联合治疗表现出持续的活性,且 AE 是在可接受范围的。
4. 多西他赛和 Abiraterone 双失败后的联合治疗
胰岛素样生长因子受体-1(IGF-1R)信号传导激活 PI3K / AKT 途径,并可能导致雄激素受体(AR)反式激活并进展为激素抵抗。xentuzumab 是一种 IGF 配体中和抗体,与 IGF-1 和 IGF-2 结合并抑制 IGF-1R 信号传导。一项研究多西他赛+Abiraterone 后进展的 mCRPC 男性随机接受 xentuzumab +恩杂鲁胺,或单独使用恩杂鲁胺的安全性和疗效。主要终点:研究者评估的无进展生存期(PFS-IA)。联合组的中位 PFS-CR 为 3.6 m,单用恩杂鲁胺组为 6.2 m(HR = 1.22 [0.70-2.13]; p= 0.48),结果相似。最常报告的 AE 是:疲劳 67% 对 49%; 食欲下降 56% 对 54%; 减重 37%vs 12%; 贫血 33% 对 44%; 背痛 30% 对 37%。结论:与恩杂鲁胺单独使用相比,向恩杂鲁胺加入 xentuzumab 并未延长 mCRPC 中的 PFS。
5. 晚期高龄前列腺癌选择顺序
在临床中经常会遇到高龄晚期前列腺癌患者的治疗选择。SIOG 指南(Droz,Eur Urol 2017)建议老年患者应接受与年轻患者相同的治疗。缺乏该患者亚群中最佳治疗顺序的证据。那么到底哪种治疗顺序会有更好的预后,下面的研究给我们一些启示。这项研究评估了在前瞻性 PROREPAIR-B 队列研究中治疗的老年人(≥ 75 岁)患者的预后。结论是不管多西他赛还是 Abiraterone/恩杂鲁胺哪个作为一线治疗,在 ≥ 75 岁的患者中,没有观察到 OS 的差异。根据治疗结果,年龄不应被视为老年 mCRPC 患者治疗选择的一个因素。
小编因为专注晚期前列腺癌方面,所以最近两次汇报篇幅较长,但也远远没有充分展示 ASCO 的魅力。后面还有肾癌和尿路上皮癌,小编也会及时向大家汇报,欢迎继续关注。