中华医学会糖尿病学分会第二十三次全国学术会议(CDS 2019)在厦门国际会展中心隆重举行。本次会议以「聚焦前沿、创新管理、注重预防」为主题,在糖尿病治疗循证医学证据专题研讨中,前任主委贾伟平教授和现任主任委员朱大龙教授分别汇报了糖尿病创新药物研发取得的成果,成为当日会上的亮点。
一、朱大龙教授:全球首创抗糖尿病治疗新药葡萄糖激酶激活剂Dorzagliatin Ⅱ、Ⅲ期临床研究

朱大龙教授就“全球首创抗糖尿病治疗新药葡萄糖激酶激活剂Dorzagliatin Ⅱ、Ⅲ期临床研究”进行汇报
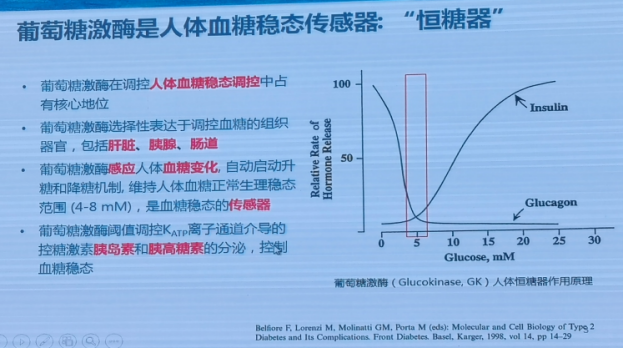
葡萄糖激酶是人体血糖稳态传感器
葡萄糖激酶在调控人体血糖稳态调控中占有核心地位,其选择性表达于调控血糖的组织器官中,包括肝脏、胰腺、肠道等。葡萄糖激酶感应着人体血糖的变化,自动启动升糖和降糖机制,以维持人体血糖正常生理稳态,是血糖稳态的传感器。其作用机制主要通过调控KATP离子通道介导的控糖激素——胰岛素和胰高糖素的分泌,从而控制血糖稳态。
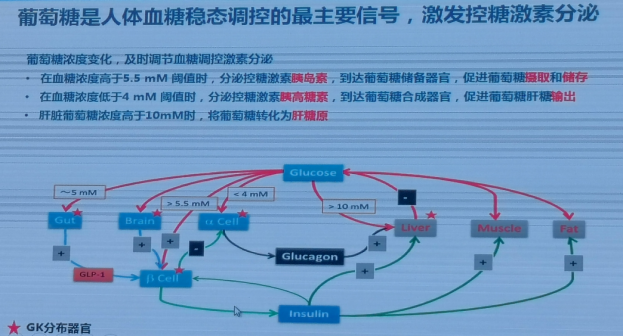
葡萄糖是人体血糖稳态调控的最主要信号,激发控糖激素的分泌:在血糖浓度高于5.5mmol/L时,分泌控糖激素胰岛素,到达葡萄糖储备器官,促进葡萄糖摄取和储存;在血糖浓度低于4mmol/L时,分泌控糖激素胰高血糖素,到达葡萄糖合成器官,促进葡萄糖肝糖输出;肝脏葡萄糖浓度高于10mmol/L时,将葡萄糖转化为肝糖原。
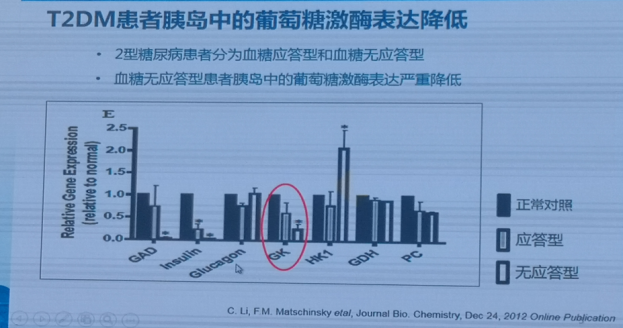
而在T2DM患者中,葡萄糖激酶表达降低,尤其是血糖无应答型患者的葡萄糖激酶表达更是严重降低。而葡萄糖激酶表达越低,糖化血红蛋白(HbA1c)越高,空腹血糖也越高。
全球首创葡萄糖激酶双重激活剂Dorzagliatin的特点及前期结果
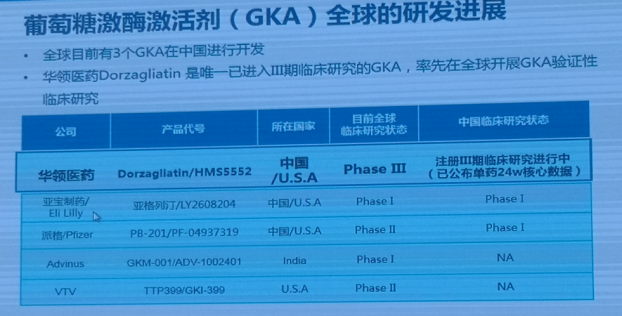
葡萄糖激酶激活剂作为治疗糖尿病新药成为近年的研究热点,目前全球共有3个葡萄糖激酶激活剂在中国进行开发,而华领医药原研创新药Dorzagliatin是唯一已经进入Ⅲ期临床研究的葡萄糖激酶激活剂。
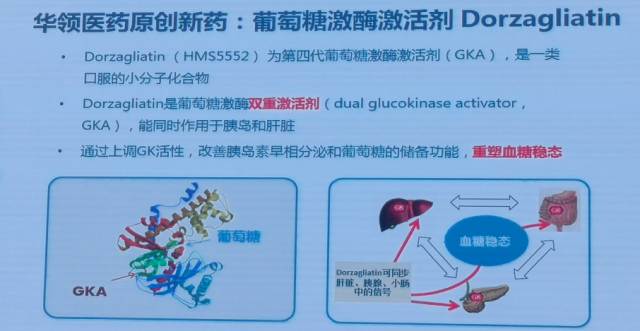
Dorzagliatin(HMS5552)为第四代葡萄糖激酶激活剂,是一类口服的小分子化合物,作为全球首创的葡萄糖激酶双重激活剂,可同时作用于胰岛和肝脏,通过上调GK活性,改善胰岛素早相分泌和葡萄糖的储备功能,重塑血糖稳态。
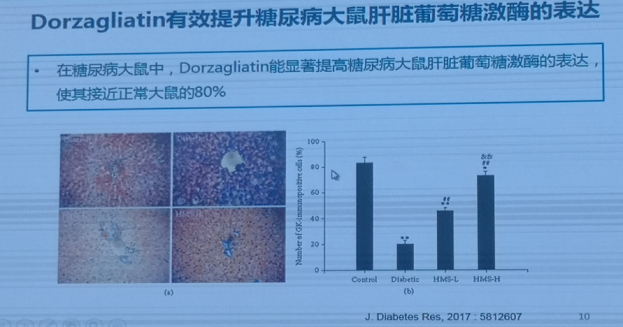
在动物实验中,Dorzagliatin可显著提高糖尿病大鼠胰岛素分泌细胞的数量和肝脏葡萄糖激酶的表达,恢复肝脏GK的表达至正常水平的80%。4项I期临床研究结果显示,Dorzagliatin能明显降低2型糖尿病患者的餐后和空腹血糖,有效控制24小时血糖,可改善胰岛素早相分泌和胰岛素抵抗,具有优异的人体药代动力学和酶动力学特征以及良好的安全性。
Dorzagliatin Ⅱ~Ⅲ期临床研究结果公布
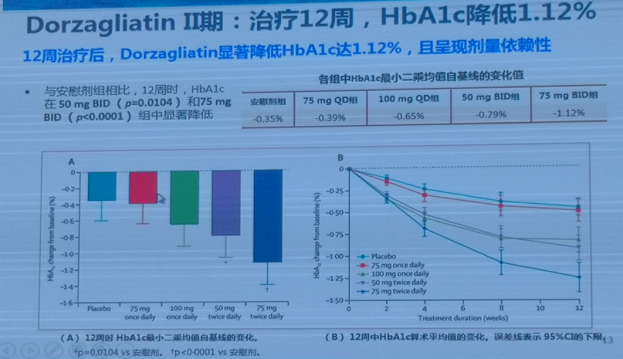
2018年5月Dorzagliatin 的Ⅱ期临床研究结果发表在Lancet Diabetes Endocrinol杂志上,并被特设专栏评述,广受国外专家好评。其研究结果表明,在经过12周的治疗后,与安慰剂组相比,Dorzagliatin可显著降低HbA1c达1.12%,且呈现剂量依赖性。
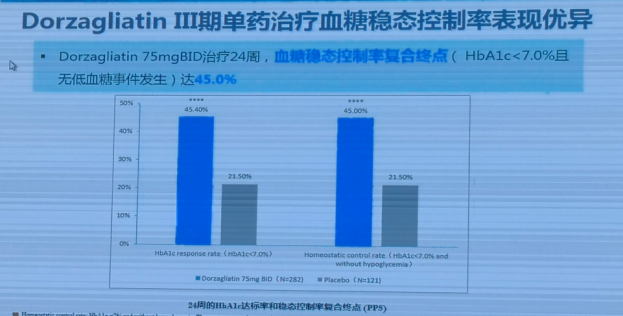
Dorzagliatin组HbA1c达标率和复合终点表现优异。在治疗结束后1周,即13周时,Dorzagliatin 75mg bid组中未用药患者的DI(处置指数)和HOMA-IR评分仍然显著改善,提示Dorzagliatin疗效具有持续性。
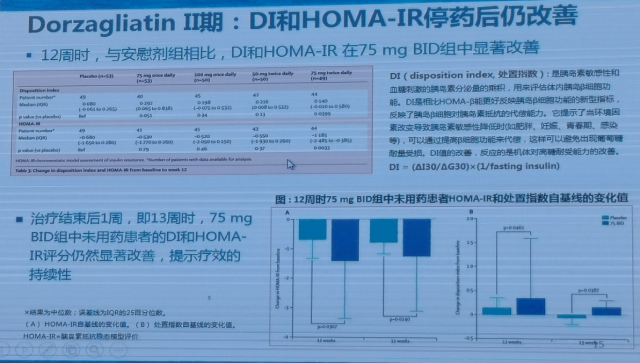
目前Dorzagliatin单药Ⅲ期临床研究已达到主要疗效终点,其结果显示:Dorzagliatin单药治疗24周HbA1c相对基线降低1.07%。
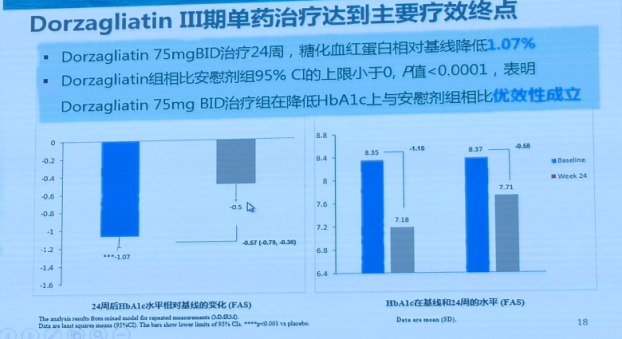
血糖稳态控制率复合终点(治疗HbA1c<7.0%且无低血糖事件发生)达到45.0%,均显著优于安慰剂组(P<0.0001)。
在24周的治疗期间内Dorzagliatin的耐受性和安全性良好,未出现死亡事件、药物相关的严重不良事件及严重低血糖(低血糖发生率低于1%)。
Dorzagliatin的其他探索性发现
目前Dorzagliatin 24周的其他研究结果及28周开放治疗的安全性研究仍在进行中。基于HMM0201临床研究数据,研究者通过深层次多维度分析,使用机器学习的方式将2型糖尿病分为6型,以期进一步分析不同分型的受试者在HbA1c、FPG、PPG 、HOMA-IR和HOMA-β改善的差异,而该分型会根据Dorzagliatin的后续研究数据进行持续的调整。
二、贾伟平教授:西格列他钠在新诊断2型糖尿病患者中的疗效与安全性评价Ⅲ期临床试验

贾伟平教授汇报西格列他钠在新诊断2型糖尿病患者中的疗效与安全性评价Ⅲ期临床试验结果
西格列他钠Ⅲ期临床试验总体设计
西格列他钠Ⅲ期临床试验是一项多中心、随机、双盲、安慰剂/阳性药平行对照试验。入组标准:运动饮食无法有效控制血糖,糖化血红蛋白(HbA1c)水平在7.5%-10%,未接受过药物治疗的2型糖尿病(T2DM)患者。安慰剂对照试验组(CMAP)由北京大学人民医院纪立农教授牵头,纳入26家中心共535例患者,在治疗24周之后,又进行了延长治疗,总的治疗周期为52周;阳性药对照试验组(CMAS)由贾伟平教授牵头进行,纳入33家中心共740例患者,对照药物为西格列汀。
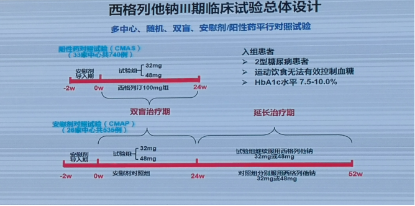
两项试验及各组间入组患者基线特征均衡可比。
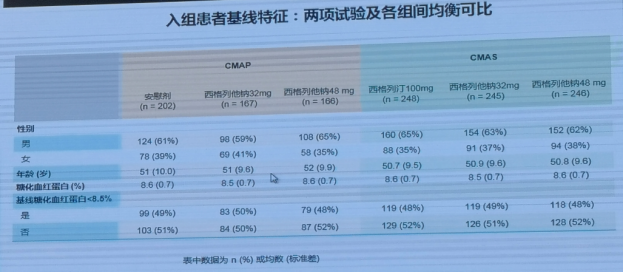
西格列他钠疗效
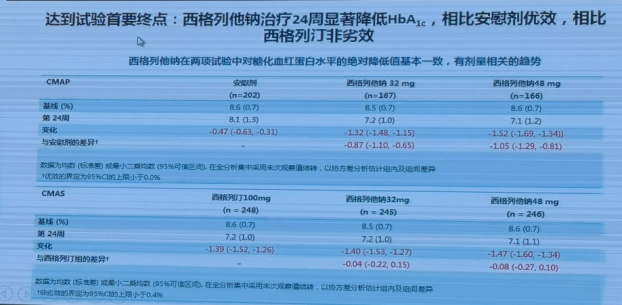
两项试验达到首要终点,西格列他钠片32mg和48mg能够有效降低HbA1c,治疗24周相比安慰剂优效,相比西格列汀片100mg为非劣效。
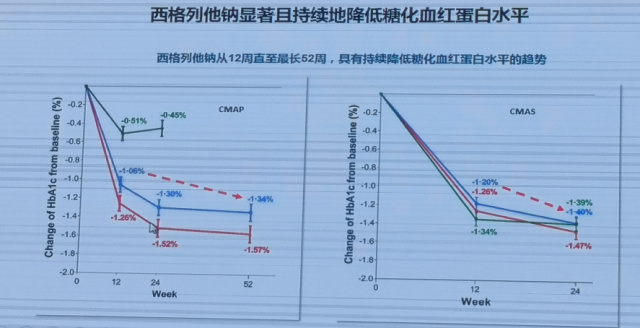
在两项试验中,西格列他钠显著且持续地降低HbA1c水平,从12周直至最长52周,西格列他钠具有持续降低HbA1c水平的趋势。
西格列他钠在两项试验中均能显著改善胰岛素抵抗,带来更好的血糖控制。

西格列他钠48mg可以明显降低甘油三酯水平。
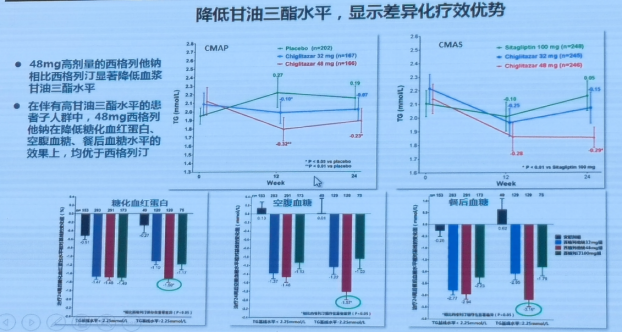
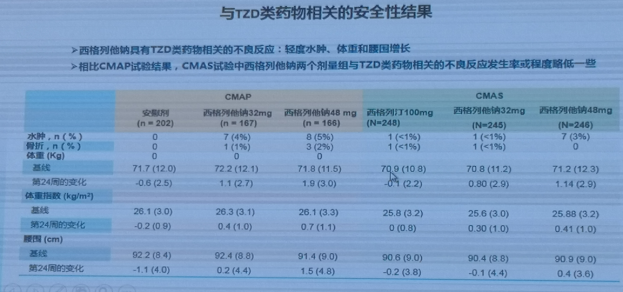
西格列他钠安全性
西格列他钠片的整体安全性良好,大多数患者对本品具有良好的耐受性和服药依从性。再24周内可出现体重增加和水肿,但其发生率和程度相对较轻。
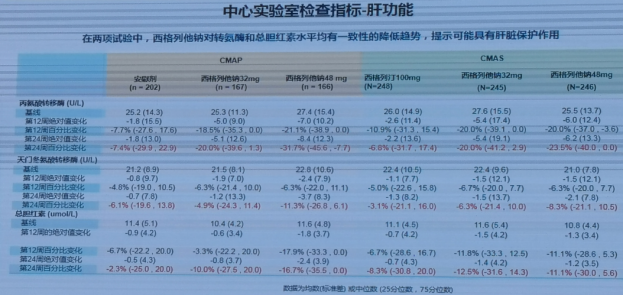
西格列他钠对转氨酶和总胆红素水平均有一致性的降低趋势,提示可能具有肝脏保护作用,但是还需要更多的临床证据支持。
领域价值
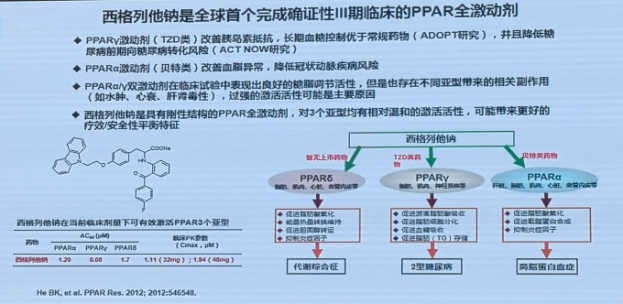
西格列他钠是全球首个完成确证性Ⅲ期临床试验的PPAR全激动剂;在两项临床试验中均没有发现在既往PPAR双激动剂临床试验中发生率较高的靶点相关副作用(水肿、肌酐水平升高),没有心衰事件发生,提示了全激动剂带来的临床疗效-安全性差异化特征;西格列他钠作为PPAR全激动剂为T2DM患者提供了一个新作用机制口服药物的治疗选择,针对存在严重胰岛素抵抗或甘油三酯水平较高的患者可能具有更好的疗效,在其他糖尿病并发症的治疗管理上也具有潜在的研究应用价值。